Отек Квинке: приобретенный и наследственный, как выявить и вылечить
С аллергическими реакциями в жизни встречается почти каждый человек, одним из ее проявлений является отек Квинке.
Отек Квинке-это реакция, которая проявляется отеком мягких тканей (кожа, слизистые оболочки, подкожно-жировая клетчатка, ткань под слизистой оболочкой).
В большинстве случаев реакция проявляется легким отеком. Но если реакция развивается быстро, отечность сильная и находится в области носа, горла, во рту, и приводит к остановке или угнетению дыхания, то необходима неотложная медицинская помощь.
Симптомы
Ниже будут перечислены симптомы отека Квинке:
- Видимы отек ткани;
- Боль и зуд в месте отека;
- Потеря чувствительности, покалывание в области отечности, связанное со сдавлением нервов;
- На отекшей ткани может появиться крапивница;
- При локализации в области дыхательных путей появляются хрипы, затруднение или остановка дыхания.
Отек Квинке возникает, когда жидкость из кровотока попадает в ткани и это приводит к их увеличению. Точная причина зависит от типа отека.
(Видео: Отёк Квинке: как спасти жизнь аллергика! Обзор, симптомы, диагностика, лечение, профилактика.)
Виды аллергической реакции
Существует два вида этой аллергической реакции:
Приобретенный
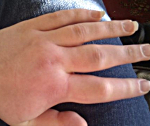
Приобретенный отек Квинке обычно вызван аллергическим ответом организма при контакте с аллергеном. Также известно, что приобретенная реакция является неспецифическим ответом организма на применение препаратов для лечения артериальной гипертензии, ингибиторов АПФ. Чаще возникает на лице, но может появляться на руках и других частях тела.
Когда в организм попадает аллерген, высвобождаются вещества, которые привлекают клетки крови к месту соприкосновения с ним. Эти вещества также вызывают увеличение просвета сосудов и их проницаемость.
Это позволяет лейкоцитам, которые обычно содержатся в стенках сосудов просочиться в ткань и бороться с аллергеном. Однако это же и позволяет проникнуть в ткань и плазме, которая и вызывает отек. Своего пика отечность достигает в течение 12-36 часов., и обычно не требует госпитализации.
Наследственный
Наследственный отек является генетическим заболеванием. Существует три типа отека и все они вызваны дисфункциональными генетическими мутациями. При всех типах возникает недостаток или отсутствие С1 ингибитора.
Основная роль С1 ингибитора заключается в уменьшении аллергического ответа иммунной системы. Недостаточное количество С1 ингибитора аллергические реакции становятся неестественными и могут возникать без причины.
Наследственный отек Квинке может возникнуть в любом месте и не ограничивается только лицом и руками. При этом заболевании может возникнуть отек в брюшной полости, вызывая боль, рвоту и диарею, а также генерализованную сыпь. Симптомы длятся 1-5 дней.
Лечение
Лечение отека Квинке заключается в том, чтобы остановить аллергию, блокируя одно из двух химических веществ, участвующих в аллергическом ответе: гистамин и брадикинин.
Приобретенная болезнь Квинке лечится антигистаминными препаратами (Зиртек, Кларитин)
Лечение наследственного отека заключается на поддержании функции дыхания и облегчении симптомов. Поскольку в реакции участвует брадикинин, а не гистамин, то препараты для лечения приобретенного отека не действуют.
Вот некоторые способы лечения наследственного отека:
- Переливание свежей замороженной плазмы.
- Инфузия ингибитора С1.
- Кальбитор. Недавно разработанный препарат, который уменьшает образование брадикинина.
- При тошноте и рвоте, диарее требуется симптоматическое лечение.
В любом случае, если симптомы возникают впервые, то необходимо обратиться к врачу. Это заболевание требует квалифицированного лечения и наблюдения.
источник
Наследственный ангионевротический отек
Наследственный ангионевротический отек – генетическое заболевание, при котором наблюдается дефицит ингибитора С1-компонента комплемента. Симптомами являются рецидивирующие отеки кожи, слизистых оболочек и органов брюшной полости, которые могут сопровождаться удушьем (при отеке гортани), рвотой и болями в животе (при поражении брюшной полости). Диагностика производится на основании осмотра, изучения наследственного анамнеза, определения С1-ингибитора, компонентов С4 и С2 в плазме крови, молекулярно-генетических исследований. Лечение осуществляется путем компенсирования абсолютного или функционального дефицита С1-ингибитора, применения блокаторов брадикинина и калликреина, использования свежезамороженной донорской плазмы.
Общие сведения
Наследственный ангионевротический отек (НАО) – вариант первичного иммунодефицита, обусловленный нарушением ингибирования системы комплемента, точнее, его основной фракции С1. Впервые это состояние было описано в 1888 году У. Осиером, который выявил рецидивирующие отеки у молодой женщины, а также установил, что подобное заболевание имелось как минимум у пяти поколений ее семьи. Примечательно, что собственно ангионевротический отек был открыт И. Квинке всего за 6 лет до обнаружения наследственной формы этой патологии – в 1882-м году. Наследственный ангионевротический отек имеет аутосомно-доминантный характер передачи и с одинаковой частотой поражает как мужчин, так и женщин. По некоторым данным, у женщин заболевание протекает тяжелее и возникает раньше, однако достоверных исследований по этому поводу не производилось. Встречаемость наследственного ангионевротического отека, по всей видимости, значительно варьирует у разных этнических групп, что дает весьма неоднородные цифры этого показателя – от 1:10 000 до 1:200 000.
Причины наследственного ангионевротического отека
Непосредственной причиной развития наследственного ангионевротического отека является первичный иммунодефицит, заключающийся в дефиците или функциональной неполноценности ингибитора эстеразы одного из компонентов комплемента – С1. В результате этого также нарушается ингибирование активации других компонентов этой системы – С4 и С2, что приводит к еще большему расстройству работы данного иммунного механизма. Врачам-генетикам удалось установить ген, отвечающий за 98% форм наследственного ангионевротического отека – им является C1NH, расположенный на 11-й хромосоме и кодирующий вышеуказанный ингибитор эстеразы С1. Различные мутации способны приводить к неодинаковым по своему течению формам заболевания, которые обладают достаточно сходными клиническими проявлениями, но различаются при проведении ряда диагностических тестов.
При одних типах мутации гена C1NH происходит полное прекращение синтеза белка-ингибитора С1, в результате чего он отсутствует в плазме крови, а остановка системы комплемента производится малоэффективными побочными путями. В других случаях наследственный ангионевротический отек возникает на фоне нормального содержания ингибитора в крови, при этом генетический дефект C1NH приводит к нарушению структуры активного центра данного фермента. В результате ингибитор С1 становится функционально неполноценным, что и служит причиной развития патологии. Существуют также редкие формы наследственного ангионевротического отека, при которых не наблюдается как изменений количества или активности ингибитора эстеразы С1, так и мутаций в гене C1NH – этиология и патогенез таких заболеваний на сегодняшний день неизвестны.
Остановка ингибирования активности компонентов комплемента (С1, С2, С4) приводит к запуску иммунной реакции, сходной по своему течению с аллергической, особенно крапивницей. Компоненты комплемента способны расширять кровеносные сосуды глубоких слоев дермы, повышать проницаемость их стенок, что провоцирует диффундирование компонентов плазмы крови в межклеточное пространство тканей кожи и слизистых оболочек и приводит к их отеку. Кроме того, немаловажную роль в патогенезе наследственного ангионевротического отека играют вазоактивные полипептиды – брадикинин и калликреин, которые еще больше увеличивают степень отека, а также способны вызывать спазм гладкомышечной мускулатуры органов желудочно-кишечного тракта. Эти процессы обуславливают все разнообразие симптомов наследственного ангионевротического отека: отечность кожи (в области конечностей, лица, шеи) и слизистых оболочек (ротовой полости, гортани, глотки), боли в животе и диспепсические расстройства, провоцируемые сочетанием отеков и спазмов.
Классификация наследственного ангионевротического отека
Всего на сегодняшний день выявлено три основных типа наследственного ангионевротического отека. Их различия в плане клинического течения патологии очень незначительны, для определения формы заболевания используют специальные диагностические методики. Врачу-иммунологу крайне важно выяснить тип наследственного ангионевротического отека, так как от этого во многом зависит тактика лечения данной патологии:
- Наследственный ангионевротический отек 1-го типа (НАО-1) – является наиболее распространенной формой заболевания, регистрируется у 80-85% больных с такой патологией. Причиной НАО этого типа является отсутствие гена C1NH или нонсенс-мутация в нем, в результате чего ингибитор С1 не образуется в организме.
- Наследственный ангионевротический отек 2-го типа (НАО-2) – более редкая форма патологии, выявляется лишь у 15% больных. Обусловлен также генетическим дефектом в C1NH, однако при этом экспрессия белка-ингибитора С1 не останавливается, а сам фермент имеет измененную структуру своего активного центра. Это приводит к его неполноценности, и он становится неспособен правильно выполнять свои функции.
- Наследственный ангионевротический отек 3-го типа – относительно недавно обнаруженная форма заболевания с практически неизученными этиологией и патогенезом. Достоверно удалось выяснить, что при этом типе отека отсутствуют мутации гена C1NH, сохраняется нормальное количество ингибитора эстеразы компонента комплемента С1 и его функциональная активность. Больше никаких данных по поводу данной формы (или их совокупности) наследственного ангионевротического отека не имеется.
Симптомы наследственного ангионевротического отека
Как правило, при рождении и в детском возрасте (за исключением редких случаев) наследственный ангионевротический отек ничем себя не проявляет. Довольно часто первые признаки заболевания возникают в подростковом периоде, так как их провоцируют стрессы и гормональные перестройки, происходящие в организме в это время. Однако нередко наследственный ангионевротический отек появляется позже – в возрасте 20-30 лет или даже у пожилых лиц. Чаще всего развитию первого приступа предшествует какое-либо провоцирующее явление: мощный эмоциональный стресс, серьезное заболевание, хирургическое вмешательство, прием некоторых лекарственных средств. В дальнейшем «порог чувствительности» по отношению к провоцирующим факторам снижается, приступы возникают все чаще – наследственный ангионевротический отек приобретает рецидивирующий характер.
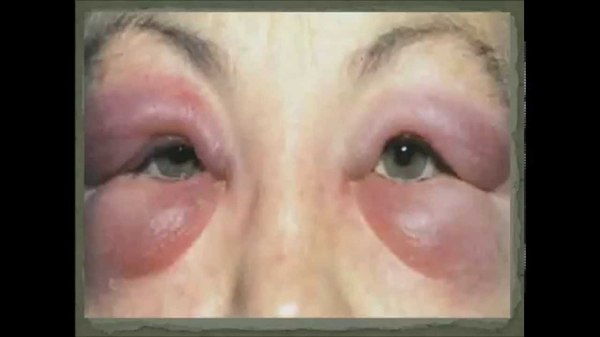
Основным проявлением заболевания у большинства больных является отек кожи и подкожной клетчатки на кистях, стопах, иногда лице и шее. В более тяжелых случаях отечные явления возникают на слизистых оболочках полости рта, гортани и глотки – при этом может развиваться удушье (асфиксия), являющееся наиболее частой причиной смерти от наследственного ангионевротического отека. В других случаях на первый план выступают симптомы со стороны желудочно-кишечного тракта: тошнота, рвота, боли и рези в животе, иногда подобная клиническая картина приобретает черты «острого живота». В отдельных случаях наследственный ангионевротический отек характеризуется сочетанием отека кожи, слизистых оболочек и поражения желудочно-кишечного тракта.
Диагностика наследственного ангионевротического отека
Для выявления наследственного ангионевротического отека используют данные физикального осмотра больного, изучения его наследственного анамнеза, определения в крови количества ингибитора С1, а также компонентов комплемента С1, С2, С4, и молекулярно-генетических исследований. Осмотр в фазу обострения заболевания выявляет отек кожи или слизистых оболочек, пациенты могут жаловаться на боли в животе, рвоту, диарею. В крови при наличии наследственного ангионевротического отека 1-го типа ингибитор эстеразы С1 полностью отсутствует, значительно снижены концентрации индикаторных компонентов комплемента. При 2-м типе заболевания в плазме крове может определяться незначительное количество ингибитора С1, в редких случаях его уровень соответствует норме, но соединение имеет пониженную функциональную активность. При всех трех вариантах наследственного ангионевротического отека уровень С1, С2 и С4 не превышает 30-40% от нормы, поэтому этот показатель является ключевым в диагностике данного состояния.
Изучение наследственного анамнеза пациента зачастую обнаруживает наличие подобного заболевания как минимум у нескольких поколений его предков и у других родственников. Однако отсутствие признаков семейного характера патологии не является однозначным критерием, позволяющим исключить наследственный ангионевротический отек – примерно у четверти больных это состояние обусловлено спонтанными мутациями и выявляется впервые в семье. Молекулярно-генетическая диагностика осуществляется путем автоматического секвенирования гена C1NH с целью выявления мутаций. Дифференциальную диагностику следует производить с ангионевротическим отеком аллергического генеза и приобретенными формами дефицита ингибитора С1.
Лечение наследственного ангионевротического отека
Терапию наследственного ангионевротического отека разделяют на два типа – лечение для купирования острого приступа заболевания и профилактический прием препаратов для предупреждения их развития. В случае острого отека Квинке, обусловленного НАО, традиционные противоанафилактические меры (адреналин, стероиды) неэффективны, необходимо использовать нативный или рекомбинантный ингибитор С1, антагонисты брадикинина и калликреина, при их отсутствии показано переливание свежезамороженной плазмы. Начинать такое лечение нужно как можно раньше, в идеале – при самых первых приступах наследственного ангионевротического отека.
Долгосрочная профилактика заболевания производится в тех случаях, когда приступы возникают слишком часто (чаще раза в месяц), если в анамнезе имелись случаи отека гортани или удушья, либо госпитализация в реанимационное отделение. Профилактика включает в себя использование андрогенов, экзогенных (рекомбинантных или нативных) форм ингибитора эстеразы С1, антифибринолитических препаратов. При доброкачественном течении наследственного ангионевротического отека – редких приступах и их относительно быстром исчезновении – такое лечение может не назначаться. Однако накануне хирургических или стоматологических вмешательств, физических и умственных нагрузок рекомендуется краткосрочно принимать вышеуказанные средства для уменьшения риска развития приступа.
Прогноз и профилактика наследственного ангионевротического отека
В большинстве случаев прогноз наследственного ангионевротического отека относительно благоприятный в плане выживаемости – при разумном лечении и профилактике приступы возникают крайне редко и не угрожают жизни больного. При этом всегда сохраняется риск отека гортани, что может привести к асфиксии и летальному исходу. Таким больным следует не только избегать значительных физических и эмоциональных нагрузок, но и желательно иметь при себе карточку или медальон с указанием диагноза. Огромное количество смертей от наследственного ангионевротического отека было обусловлено неверными действиями медиков, не знающих диагноза и поэтому использующих традиционные при аллергическом отеке Квинке препараты, которые неэффективны при НАО.
источник
Медицинский центр
«Бене Вобис»
Выберите город — Казань?
Выберите город
Эффективное
лечение аллергии
Видеоролики об аллергии
Прошел 1 курс лечения АЛТ.Очень внимательное отношение всего персонала к пациенту!Пока никаких симптомов аллергии нет. Очень надеемся,что больше и не появится!Обязательно будем приходить сюда на повторную АЛТ!Очень понравилось отношение всех докторов,медсестер,девушек красивых в регистратуре.Это единственная клиника,где у нас обнаружили аллергию!Значит есть надежда ее вылечить!Спасибо Вам за все. До встречи!Удачи,процветания,здоровья!
Новая книга Надежды Юрьевны Логиной
«Загадки иммунитета. Как мобилизовать свою иммунную защиту и победить аллергию»
Отек Квинке ангионевротический: симптомы и лечение у детей и взрослых
Ангионевротический отёк Квинке имеет два типа согласно своему происхождению. Первый – это отек, приобретённый на генетическом уровне, то есть, наследственный, а второй – аллергический. Но и первый и второй имеют общую клинику. Отличаются тем, что наследственный ангионевротический отек является постоянным, то есть, хроническим. Это – врождённое проявление недостатка работы иммунной системы, которое зафиксировано в генетическом коде человека и передаётся по наследству.
1. 
Клиническая картина при наследственном ангионевротическом отёке выглядит в виде отёчности кожных покровов местами, подкожных тканей и слизистых. Отёчности подвергаются слизистые верхних органов дыхания, ЖКТ, мочеполовой системы.
Поскольку наследственный ангионевротический отек очень легко перепутать с отёком Квинке, то это порой приводит к ошибкам в диагностике и соответственно назначенное лечение либо не приносит ожидаемого результата, либо становится причиной серьёзных осложнений. Ведь, несмотря на схожие симптомы, профилактика и лечение существенно отличаются друг от друга.
Избежать сомнений в правильности диагноза, можно только имея в руках результаты лабораторных анализов. Только эти исследования способны отобразить реальную картину происходящего в организме – является ли отёк врождённым нарушением иммунной системы или же это реакция на аллерген.
2. Отек Квинке ещё называется гигантская крапивница и представляет собой отёчный участок кожи и подкожного слоя клетчатки, имеющий чёткие контуры. Он очень напоминает крапивницу, но в отличие от крапивницы при отёке Квинке нет зуда. Бывают случаи осложнения отёка Квинке, когда обостряется течение заболевания. В этой ситуации может ощущаться достаточно сильный зуд, который тяжело переносить.
Отек квинке у детей и взрослых: история и исследование заболевания

Спровоцировать аллергию и последствия её в виде отёка Квинке может употребление человеком в пищу некоторых продуктов питания типа морепродуктов, плодов цитрусовых, копчёностей, шоколада и кондитерских изделий (в состав которых входит тартразин, краситель). Также спровоцировать выработку гистамина способны томаты, орехи, яйца, сыр и рыба.
Довольно часто спровоцировать ангионевротический отек Квинке может привести использование антибиотиков и других лекарственных средств: обезболивающих, противовоспалительных, контрастных веществ при проведении рентгенографии. К аллергической реакции и отёчности тканей может привести употребление витаминов, инсулина, а также использование препаратов крови, содержащих белок.
Наиболее опасным последствием аллергической реакции на укусы насекомых типа пчёл, ос, шершней, является отёк гортани. Если не принять своевременные меры, то этот отёк может привести к удушью.
В отличие от аллергического отёка, псевдоаллергический отёк Квинке у детей проявляется в результате дефицита иммунитета, который к тому же усиливается присутствием в организме разных инфекций (бактериальной или вирусной при роды), паразитов, глистов, а также бактерии Helicobacter pylori. Причиной псевдоаллергического отёка также может стать нарушение микрофлоры кишечника.
Когда в течение отёка Квинке появляется волдырная сыпь (гигантская крапивница) этот процесс называют ангионевротический отёк. Места локализации этого вида отёка следующие: нижняя лицевая часть, слизистые (рот, носоглотка, верхние дыхательные пути, ЖКТ, мочеполовая система).
Ангионевротический отек: симптомы в области гортани
Если не остановить развитие отёка, то в результате удушья может наступить смерть.
Лечение ангионевротического отека
При стремительном развитии отёка Квинке необходимо предпринять срочные меры, для того, чтобы остановить его развитие.
Лечение наследственного ангионевротического отёка возможно после лабораторного подтверждения его присутствия. Но сначала понадобится обеспечить соблюдение условий, которые позволят оградить организм от некоторых факторов, провоцирующих развитие отёка. То есть, при генетической склонности к развитию НАО, необходимо
- ограничить занятия спортом и физические нагрузки, связанные с работой;
- не допускать хирургических операций;
- стараться избегать травм.
Корректно и профессионально излечить ангионевротический отек квинке можно только в больнице, поэтому при подозрении на НАО необходимо обратиться к врачу.
Основная симптоматическая терапия заключается в применении противоаллергических препаратов, а также препаратов, направленных на ликвидацию симптомов, например, успокоительных, обезболивающих и укрепляющих иммунную систему.
Новое направление в лечении отека Квинке
Довольно часто используемые медицинские препараты не приносят ожидаемого эффекта, либо же лечение приносит временное облегчение, но затем всё снова повторяется.
Но аутолимфоцитотерапия на данный момент считается одному из наиболее успешных методов лечения. Особенно важно то, что аутолимфоцитотерапия лечит гионевротический отек Квинке любого типа и происхождения.
Эффективность метода аутолимфоцитотерапии зависит не только от своевременно оказанной помощи, но и в подкожном введении собственных иммунных клеток (лимфоцитов), которое осуществляется 8-10 раз в месяц. Рекомендуется проходить данное лечение в течение одного месяца.
Аутолимфоцитотерапию называют одновременно и уникальной, и универсальной методикой лечения всех проявлений отёка Квинке в организме человека.
источник
Наследственный ангионевротический отек (последняя часть — редкие виды ангионевротического отека (не отек Квинке))
Наследственный ангионевротический отек (НАО) — хроническое заболевание, относящееся к группе первичных иммунодефицитов с аутосомно-доминантным наследованием и неполной пенетрантностью, связанное с качественным или количественным генетически детерминированным дефектом генов, кодирующих синтез ингибитора эстеразы компонента комплемента C1 (С1inh), которое проявляется в виде рецидивирующих отеков (О.) кожи и слизистых оболочек дыхательных путей, желудочно-кишечного (ЖКТ) и урогенитального трактов. Первые упоминания о подобных О. были сделаны Гиппократом в IV в. до н. э.
В настоящее время известны 3 различных дефекта, которые клинически неразличимы:
-первый — в 80–92% случаев количественный дефицит С1inh при определении иммунологическими и энзиматическими методами — НАО I типа;
-второй — в 15% случаев структурный дефект со снижением функциональной активности при нормальном или повышенном уровне С1inh — НАО II типа;
-третий — в 1–5% случаев структурно измененный С1inh (с возможным ↑ концентрации в 3-4 раза); образуются агрегаты с глобулинами (или альбумином) сыворотки крови или активность С1inh блокирована аутоантителами — НАО III типа. Основной механизм ангиоэдемы при НАО связан с эффектами медиаторов — брадикинина, гистамина, производных арахидоновой кислоты, цитокинов.
С1-ингибитор – высокогликозилированный белок сыворотки, синтезируемый в печени и угнетающий протеолитическую активность субкомпонентов Clr и Cls, предупреждает активацию С4- и С2-компонентов комплемента. Структура ингибитора С1 закодирована в хромосоме 11, этот протеин является a2-глобулином и вырабатывается преимущественно в гепатоцитах, хотя активированные моноциты, мегакариоциты, эндотелиальные клетки и фибробласты способны синтезировать его в небольшом количестве.
Основными функциями С1-эстеразы являются:
• предотвращение спонтанной активации классического каскада комплемента;
• регулирование активации каскада свертывания крови, при ингибировании факторов свертывания крови XIa и XIIa;
• ингибирование превращения плазминогена в плазмин в процессе фибринолиза;
• ингибирование активированного калликреина в реакциях калликреин-брадикининовой цепи.
При дефиците С1-ингибитора увеличивается содержание калликреина, который, в свою очередь, повышает образование брадикинина. Недостаточность С1-ингибитора приводит к неконтролируемой активации ранних компонентов комплемента. Локальный дефицит ингибитора С1 приводит к нарушению регуляции и повышению продукции вазоактивных пептидов и, соответственно, к развитию локального отека. Некоторые конечные продукты перечисленных каскадов, такие как брадикинин или компоненты комплемента, являются вазоактивными пептидами, стимулирующими повышение проницаемости капилляров и экстравазацию плазмы, а также спазм гладкой мускулатуры пищеварительного тракта и полых органов. В настоящее время обсуждается ведущая роль брадикинина в развитии симптомов комплементзависимых отеков.
1. Положительный генетический (семейный) анамнез в 70–80% случаев (на протяжении 3-4 и даже более поколений), но отрицательный наследственный анамнез не является критерием исключения диагноза НАО.
2. Особенности отека (как отличить от отека Квинке):
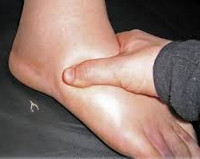
-бледный, очень плотный, имеющий четкую границу со здоровой кожей, захватывающий от 3-4 см в диаметре до больших участков;
-без гиперемии («холодные отеки»), с чувством «напряжения», «распирания тканей». Характерны болезненные отеки лица, туловища, конечностей, нередко одной и той же локализации («цикличные отеки»). При надавливании на отек ямки не остается.
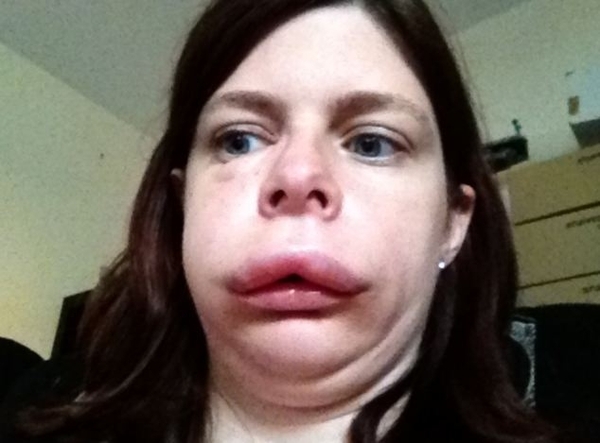
Отак Квинке (аллергический)
3. Четкая связь отека кожи и/или слизистых оболочек, абдоминалгий (болей в животе) с триггерами (провоцирующими факторами):
-механической травмой, интенсивность которой может быть самой разной — от легкого сдавления одеждой или легкого ушиба и до перелома кости (в том числе спортивные и производственные травмы);
-возникновение отека после экстракции зуба, хирургических операций, диагностических манипуляций инвазивного характера. Часто таким пациентам ставится диагноз аллергии на ВСЕ анестетики, хотя причина отека – непосредственно инъекция, неважно каким препаратом;
4. Возникновение отека кожи и/или слизистых оболочек и абдоминалгий при интенсивной физической нагрузке, охлаждении, психоэмоциональной перегрузке, на фоне инфекционных заболеваний, менструаций (часто дебют в подростковом возрасте), приеме пероральных контрацептивов, во время беременности.
5. Локализация отека: часто в области дистальных (кисти, стопы) отделов конечностей, верхних дыхательных путей (более 20% случаев) и ЖКТ (более 40% случаев).
6. Сроки развития и динамика изменений отека, течение заболевания:
-отек формируется на протяжении нескольких часов (от 1 до 36 ч)
-регрессия (саморазрешение или после лечения) в течение 10–72 ч (максимально до 7–14 дней). Характерны ремиссии от 7–10 дней до 12 мес, возможны непрерывные атаки, а также латентное (субклиническое) течение.
7. Развитие кольцевидной эритемы (erithema annulare) более чем в 50% случаев.
8. Крапивница, местная гиперемия и зуд не характерны.
9. Абдоминалгии в сочетании с ангиоэдемой или изолированно при атипичном течении.
10. Симптом «географического живота» — часто таких больных многократно оперируют по поводу острых болей в животе, удаляют аппендикс, части кишечника, женские половые органы (трубы, яичники, матку)
11. Качественный или количественный дефицит С1inh в момент приступа отека и/или абдоминалгии
12. Снижение С4-, С2-, C1-компонентов комплемента в периферической крови (наблюдается не всегда). При снижении С8, С9 возможно более тяжелое течение.
13. Периферическая эозинофилия, ↑ общего IgE, положительные скарификационные (или прик-) аллергопробы с бытовыми, эпидермальными, пыльцевыми и пищевыми аллергенами не выявляются (возможно редкое сочетание атопии и НАО).
14. Положительный выраженный эффект при в/в введении очищенного С1inh, нативной плазмы, эпсилон-аминокапроновой кислоты (Э-АКК), даназола, станазола, метилтестостерона, икатибанта.
15. Неэффективность антигистаминных препаратов, глюкокортикостероидов (эффект слабый или отсутствует), норадреналина, антибиотиков, противопаразитарных препаратов, ферментов, вегетопротекторов и дургих препаратов.
Особенности клинической картины
Первые признаки НАО могут возникнуть уже в возрасте нескольких месяцев, но чаще после 1-2 лет жизни. У большинства больных НАО дебют заболевания возникает до 20 лет (60%), гораздо реже — в среднем и даже пожилом возрасте. В пубертатном периоде течение заболевания может утяжелиться в связи с гормональной перестройкой. Больные неоднократно наблюдаются у различных специалистов и не сразу обращаются к аллергологу-иммунологу (а если обращаются, то, часто, верный диагноз не ставится годами – из моего личного опыта).
Отсутствие в семейном анамнезе сведений о НАО не исключает возможности постановки подобного диагноза. Клинические проявления у пациентов характеризуются рецидивирующими отеками различной локализации: кожи лица (губы, периорбитальная область), шеи, туловища, конечностей, слизистых оболочек верхних отделов дыхательных путей, в том числе гортани, желудочно-кишечного (приступообразные боли в животе) и урогенитального трактов. Отек может распространяться на верхние дыхательные пути с вовлечением пищевода, гортани и проявляется дисфагией (нарушением глотания), дисфонией (нарушением голоса), симптоматикой обструкции (закупорки) дыхательных путей, напоминающей в ряде случаев бронхиальную астму, и прогрессировать вплоть до асфиксии (резкое нарушение дыхания). Смертность при НАО составляет 20–30%. Больным с отеком без симптомов крапивницы и кожного зуда следует уделять особое внимание, так как у них может быть НАО с синдромом недостаточности С1inh, носящий наследственный характер.
Интервалы между обострениями у каждого больного индивидуальны: у некоторых больных отеки возникают только после значительной травмы, у других обострения проявляются через каждые 9– 14 дней, вне зависимости от внешних воздействий, на протяжении многих лет. Нередко у больных наблюдается аура в виде слабости, разбитости, мраморность кожи, обильных бледных высыпаний типа кольцевидной эритемы, сохраняющейся во время отека, не сопровождающиеся зудом, жжением и ↑ t°. Отек может возникать на любом участке кожи или слизистых оболочек.
У более половины больных наблюдаются выраженные боли в животе (вызваны отеком различных участков слизистой оболочки ЖКТ). Развитию приступов абдоминалгии при НАО часто предшествуют ощущения спазмов в околопупочной области, слабость, тошнота, спастические боли в эпигастрии. Абдоминалгия нередко сопровождается рвотой и жидким стулом, характерна болезненность живота при пальпации. Клинически болевой синдром проявляется в виде разлитой боли в брюшной полости, кишечных колик, возможна тонкокишечная непроходимость. У ряда пациентов наблюдается первичный генез рецидивирующей тонкокишечной непроходимости как forme fruste (приостановление в развитии или скрытое течение заболевания), и только исследование концентрации С4-фракции комплемента позволяет правильно поставить диагноз (далеко не всегда – из моей практики). Некоторые пациенты предъявляют жалобы на ощущения «отеков внутренних органов».
Боли в животе бывают настолько интенсивными, что их иногда называют «брюшная мигрень», а сопровождающие болевой симптом общие явления (тахикардия, колебания АД, головокружение, головная боль и др.) — «вегетативная буря». Из-за абдоминалгии больные часто подвергаются лапаротомии, при операции выявляют ограниченный отек кишечника, признаки асептического воспаления (часто ничего не выявляют, а просто удаляют органы).
В более редких случаях при локализации отека на лице могут вовлекаться менингеальные (мозговые) оболочки с проявлением менингеальных симптомов (ригидность затылочных мышц, резкая цефалгия, рвота, иногда судороги), при поражении лабиринтных систем развивается синдром Меньера, что выражается головокружением, тошнотой, рвотой. Все эти симптомы могут встречаться как одновременно, так и по отдельности. При атипичном течении отека могут отсутствовать, также возможны изолированные абдоминалгии, характерны полиартралгии, снижение С4-фракции комплемента. В очень редких случаях описаны: эпилептический приступ, уртикарии, кожная пурпура, феномен Рейно. При лабораторном обследовании больных НАО обнаруживается: С1inh обычно не более 20–30% от нормального (или отсутствие даже в период полной ремиссии), концентрации С2- и С4-компонентов — не более 30–40% от нормальных (не всегда), уровни С1 и С3 в плазме чаще нормальные. В результате нарушения ингибирования активности С1 постоянно происходит активация комплемента.
В 80-х гг. J. T. Chiu и соавт. описали редкие случаи приобретенной гипокомплементемии и приступов АНО со снижением содержания С1inh в плазме, что наблюдается при активации и потреблении комплемента при инфекционных заболеваниях и обострении болезней, обусловленных циркуляцией «иммунных комплексов» (ЦИК). Известно редкое явление — персистирующий приобретенный дефицит С1inh в сочетании с ↓ содержания С1, С4 и С2 у больных В-клеточными лимфомами.
По сравнению с врожденной формой, приобретенный АНО (ПАНО) с дефицитом С1inh, встречается реже, при этом у других членов семьи больного не обнаруживаются аномалии уровня С1inh. Это комплемент-зависимый ПАНО связан с ускорением метаболизма С1inh в 2-3 раза.
Кроме ↓ уровня С4 и С1inh для больных с приобретенной формой заболевания характерно ↓ С1 и С1q, что помогает проводить дифференциальную диагностику. ПАНО можно отличить от НАО по отсутствию дефектности системы комплемента у здоровых родственников и ↓ содержания С1-компонента, при наследственной форме обычно содержащегося в нормальном количестве.
Рекомендации по лечению и ведению пациентов при НАО
Пациенты с НАО требуют не только дифференцированного индивидуального подхода, но и назначения препаратов, учитывая возможный риск, изменение качества жизни. Такие предпосылки обусловлены тем, что дебют заболевания чаще происходит в пубертатный период, когда имеются не только эндокринные, но и психологические проблемы у пациентов с НАО.
В случае дебюта НАО у девочек в пубертатном периоде или женщин во время беременности и лактации рекомендуется начинать лечение с введения нативной плазмы.
Обязательный прием даназола (дановала) (НАСКОЛЬКО ЗНАЮ НА ДАННЫЙ МОМЕНТ ПРАКТИЧЕСКИ НЕТ В РОССИИ, нашла цену в интернете около 15 000 за 60 капс по 200мг) постоянно, по жизненным показаниям, ежедневно по схеме: 200 мг 3 раза в день (600 мг) в течение 10–14 дней, затем 200 мг в день (по 1 табл. 2 раза в сутки) 1 мес, 100 мг/сут 6 мес, изменение дозы возможно под контролем аллерголога. Или прием метилтестостерона (купить Метилтестостерон достаточно сложно, так как препарат отсутствует в свободном обороте, нашла цену около 50 $ за 100 таб 25 мг) в начальной дозировке 0,01 г (по 0,005 г 2 раза в сутки, сублингвально; максимальная суточная доза составляет не более 0,025 г) ежедневно. Контроль в крови комплемента для коррекции дозы даназола.
В период обострения НАО, при отеке жизненно важных органов: свежезамороженная (или свежая) нативная (хранение плазмы при -30°С возможно не более 2 мес) или 5% р-р Э-АКК. Для купирования острых отеков введение Э-АКК менее эффективно, чем нативной плазмы.
Вместо Э-АКК можно использовать транексамовую кислоту 1-1,5 г внутрь 2-3 раза в день.
Так же для купирования отека высоко эффективен препарат Фиразир (для однократного введения требуется 3 мл (1 ампула), цена за ампулу около 150 000 руб)
Для лечения острых приступов применяют очищенный концентрат С1inh 3000 — 6000 ЕД 1-2 ампулы. Рекомендуется применять очищенный С1inh не менее 3 раз в год. К сожалению, препарат С1inh дорогостоящий и не зарегистрирован в РФ, поэтому не может рекомендоваться для широкого использования в нашей стране.
При отеке гортани ингаляционно 0,1% р-р адреналина, 5% р-р эфедрина, В-адреностимуляторы, госпитализация в ЛОР-отделение.
При развитии абдоминального синдрома — наблюдение хирурга. При выраженных болях, рвоте, поносе необходимо введение анальгетиков и спазмолитиков (баралгин, платифиллин, но-шпа и др.) под постоянным наблюдением хирурга, так как длительно существующий отек стенки кишечника может вызвать некроз и потребовать оперативного лечения.
Больным с относительными противопоказаниям (обычно при невозможности купить) к приему даназола и метилтестостерона прием Э-АКК 4–12 г/сут под контролем свертывающей системы крови каждые 10–14 дней.
Следует избегать нахождения и работ в сырых, запыленных помещениях, психоэмоциональных нагрузок. Противопоказаны интенсивная физическая нагрузка, механическое воздействие на кожу и слизистые оболочки. Своевременная санация очагов хронической инфекции. Лечение антибиотиками строго по показаниям и по назначению врача, с определением чувствительности микрофлоры, при необходимости, применение противогрибковых средств.
Исключить препараты пенициллинового ряда и их производные, В-блокаторы, фитопрепараты, ингибиторы АПФ.
Динамическое наблюдение аллерголога-иммунолога, других специалистов по показаниям.
Пациенты с НАО нередко нуждаются в психологической и социальной реабилитации (конечно, когда по 15-20 лет не был установлен диагноз, а, если повезло и установили, невозможно купить препараты для лечения).
Для многих пациентов зрелого возраста характерно многолетнее и безуспешное лечение у врачей различных специальностей — терапевтов, гастроэнтерологов, гинекологов, хирургов, врачей приемных комиссий военкоматов и др. В связи с этим больным НАО часто ставят неправильный диагноз (отек Квинке, крапивница, аллергия, острый живот, острый аппендицит, острый холецистит, стеноз чревного ствола, ангина, ревматологическое заболевание, кровоизлияние в мозг, мигрень, эпилепсия и др.) и назначают неадекватную для данного заболевания терапию, что становится причиной высокой смертности таких пациентов. Около 25% больных умирают от О. гортани в возрасте до 30 лет. Многим больным неоднократно проводят лапаротомии и трахеотомии из-за некупирующихся отеков.
Случай из моей практики (простите за капс):
Я встерилась с НАО в первые пол года работы аллергологом. В мой кабинет зашла женщина с отеком лица, котрый мне сразу показался странным и непохожим на отек Кивнке, а похожим как раз на НАО. Поскольку отек мне показался таковым, я начала более тщательно собирать анамнез и он пошел как по учебнику. Все критерии, описанные выше, совпали, ВСЕ! При этом пациентка страдала отеками с 13 лет (на момент обращения ей было 45-46 лет), консультирована ВСЕМИ аллергологами моего города, в том числе и ведущим аллергологом края. ДИАГНОЗ НАО НЕ БЫЛ УСТАНОВЛЕН И ДАЖЕ ЗАПОДОЗРЕН! Пациентка многократно была пролечена стероидами и антигистаминными препаратами безуспешно. Я, заподозрив НАО, бегу к своему заведущему, он смотрит и говорит – очень похоже. Госпитализируем, капаем гамма-аминокапронку, отек купируется за 2 суток. До этого на «стандартном» лечении отек длился до 7-10 дней.
Этот случай был первым в нашем отделении и явился пусковым моментом для налаживания диагностики и лечения НАО у нас. Для лабораторного подтверждения НАО требуется анализ на уровень и функциональную активность С1-ингибитора. Реагенты для этого анализа не зарегистрированы в России для применения в клинической практике. Существует одна лаборатория в Москве, которая проводит этот анализ, у них реагенты зарегистрированы для применения в научных целях. Мой заведующий нашел ее, связался и договорился об отправке плазмы крови таких больных к ним на анализ. Эта пациентка была первой в истории моего города, которой был проведен данный анализ и результат 100% подтвердил данный диагноз. НАО находится в списке орфанных заболеваний, лечение которых финансируется государством. Единственное, что мы смогли для нее «выбить» — это бесплатно получение гамма-аминокапроновой кислолты. Так же мой заведующий убедил главврача закупить препарат Фиразир для экстренной помощи больным НАО. На данный момент в нашем городе он имеется только у нас.
Сейчас у нас под наблюдением находится 4 пациента с подтвержденным диагнозом НАО!
источник